mRNA癌症疫苗按下加速键,国内企业比学赶超进展如何?
据美柏医健刊文,从1960年mRNA首次被成功提取,60多年后通过改造mRNA得到具有划时代意义的mRNA新冠疫苗,mRNA技术才真正发挥巨大作用。要不是因为一位女科学家的坚持,这项技术或许还要很久才会被关注。
不过,虽然以疫苗产品闻名,但mRNA技术的未来远不止于此。
今年10月,BioNTech的两位创始人在接受BBC采访时表示,基于mRNA疫苗技术路线的癌症疫苗研究已经取得了突破,有望于2030年前问世。如果mRNA技术发展能够顺利,那么人类离治愈癌症可能不远了。

▲来源:http://biosmedi.com/index.php?m=home&c=View&a=index&aid=65
1从边缘到舞台中央
1985年,匈牙利生物研究员卡塔琳·卡里科因迟迟没有研究成果而被匈牙利科学院生物研究中心解雇。痴情于mRNA的她原本想在欧洲找到一份继续研究的工作,却接连遭遇挫败。无奈之下,卡塔琳·卡里科转战美国,却仍然屡屡碰壁。
1995年,由于持续性地无法申请到项目基金,在宾夕法尼亚工作六年后的卡塔林·卡里科被降职,错失成为该校全职教授的机会。直至1997年加入同样坚信mRNA技术的免疫学家德鲁·魏斯曼的团队,卡塔林·卡里科的研究才开始出现转机。

▲德鲁·魏斯曼(DrewWeissman)和卡塔林·卡里科(KatalinKarikó)来源:参考资料1
在卡塔林·卡里科之前的研究过程遇到的最大的瓶颈是,不管是天然RNA还是在体外人工合成的RNA,都会毫无例外地激活人体免疫细胞的反应,从而导致RNA还没来得及被翻译成蛋白质就降解了。2005年在德鲁·魏斯曼的协助下,卡塔林·卡里科发现对RNA组成成分之一的尿苷修饰后的mRNA都可逃避免疫传感器的信号识别,从而解决了RNA应用研究中最大的难题。这一突破性的研究发表在了 Immunity 杂志上,这也标志着RNA疗法的诞生。
2007年,哈佛大学医学院的助理教授德里克·罗西通过使用卡塔林·卡里科和德鲁·魏斯曼修饰mRNA尿苷的方法在干细胞上进行RNA的应用研究,尝试将体细胞重编程为胚胎样干细胞。在经过一年多的探索后,他们成功了。2010年,这一研究被《时代》杂志评为当年的十大医学突破之一。
很快,德里克·罗西便成立了Moderna公司。
在德国,一对土耳其科学家夫妻乌古尔·萨欣和奥兹朗·图雷利早早就关注到了卡塔林·卡里科和德鲁·魏斯曼的研究,也迅速地创立了基于mRNA疗法的生物技术公司——BioNTech。

▲BioNTech创始人乌古尔·萨欣和奥兹朗·图雷利?来源:参考资料4
往后的故事,大家都已经耳熟能详。疫情之下,mRNA疫苗成为全球最大的医药品类。2021年,BioNTech的BNT162b2疫苗和Moderna的mRNA-1273疫苗分别创下404亿美元和176.75亿美元的营收,成为全球销售额第一和第三的医疗产品。
然而,mRNA疫苗治疗癌症仍然面临很多挑战,比如识别肿瘤特异性表位仍然是一个长期需要探索的问题,比如如何验证最可行的给药方式等。
2必须突破的挑战
mRNA癌症疫苗可分为两类,包括基于树突状细胞(DC)给药的mRNA疫苗和直接注射的mRNA疫苗。
DC疫苗通过体外转录获得mRNA,转染至DC后,mRNA在细胞质中翻译形成抗原从而激活DC,将激活的DC注入人体以激发免疫系统应答,达到杀死肿瘤细胞的目的;直接注射的mRNA疫苗则是以粒细胞-巨噬细胞集落刺激因子(GM-CSF)作为佐剂,将编码相关抗原的mRNA注射入患者体内,从而刺激机体产生抗体,抑制肿瘤细胞生长。
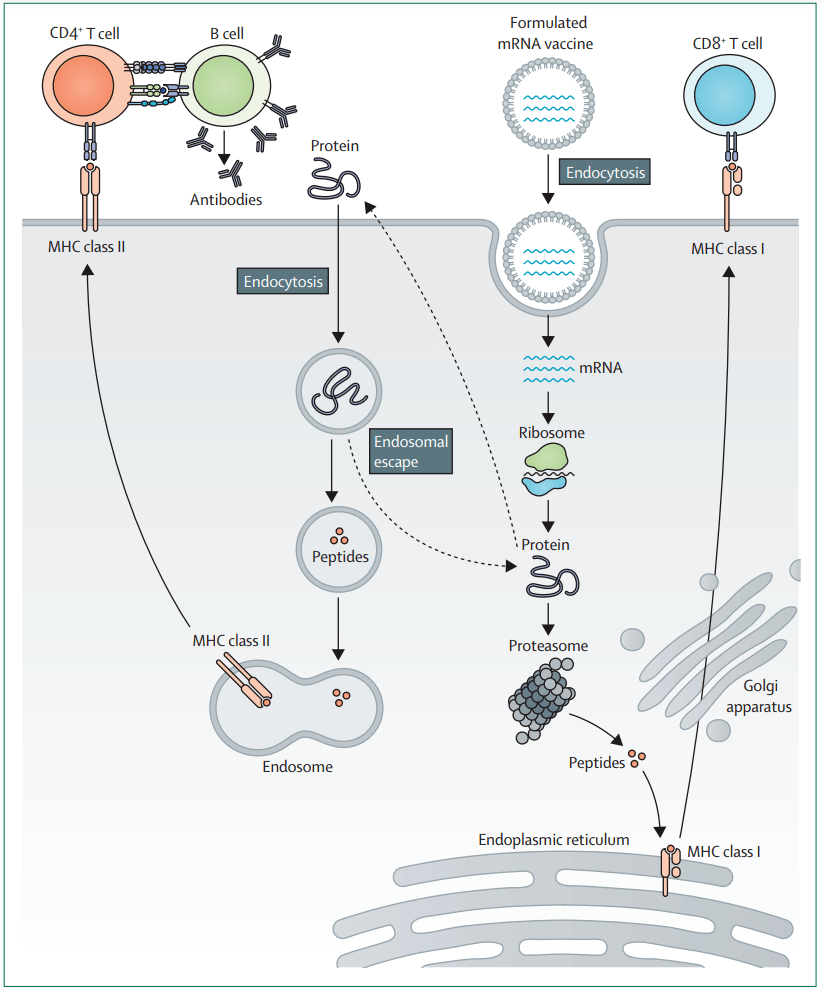
▲基于mRNA的疫苗作用模式?来源:参考资料3
1996年,第一个基于mRNA的癌症疫苗研究首先在DC中进行了体外实验。如今,科学技术的进步使mRNA的结构、稳定性、注射方式得到多方面优化。mRNA可以通过皮内、皮下、鼻内、结节内、肌肉内、瘤内和静脉注射等方式进行给药。如何将其成功的递送到人体成了mRNA技术发展的最大挑战。
mRNA由单链构成,很容易在人体内发生降解;同时,mRNA想要实现翻译功能必须进入到细胞膜内,但由于mRNA和细胞膜均带负电荷,会产生排斥反应,导致mRNA难以进入。受这些因素阻碍,即使mRNA不会引起免疫反应,但仍难以起到安全稳定的治疗目的。
为了促进细胞对mRNA的摄取,科学家开始尝试利用递送系统来辅助。为了提高递送效率并尽可能降低治疗副作用,研究者开发了多种包裹mRNA的递送载体。递送mRNA疫苗的手段有物理方法、病毒载体方法和非病毒载体方法。脂质体及其衍生物已成为目前递送mRNA最有效的非病毒载体。用于递送mRNA疫苗的脂质载体主要分为以下几种:脂质体复合物(LP);脂质体聚合物(LPR);脂质体纳米粒(LNP);阳离子纳米乳(CNE)。
目前三种mRNA新冠疫苗均采用了LNP递送系统。
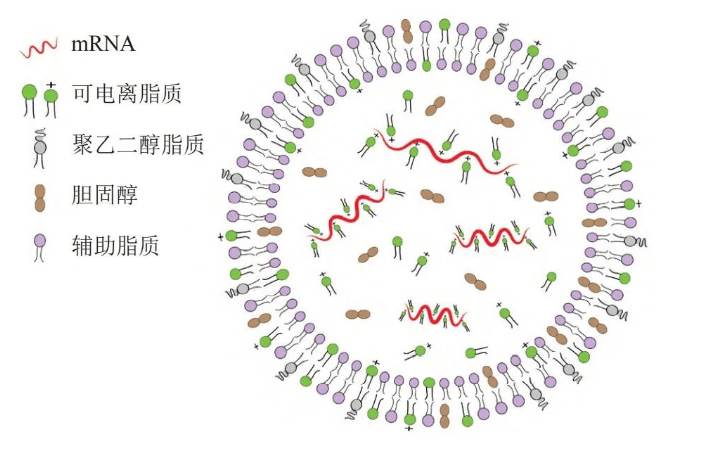
LNP通常包括四种成分,可电离脂质/可离子化脂质、胆固醇、辅助磷脂/中性脂质、PEG修饰脂质,它们共同封装和保护脆弱的mRNA。不同分子及构成比例是各家LNP系统的主要差异所在。
但以LNP为载体制备的mRNA制剂会在肝脏及脾脏聚集,难以靶向其他部位,并易发生渗漏,在很大程度上限制其作为药物载体的应用。行业也正在探索脂质复合物、多聚体等新型递送载体。
聚合物和聚合物纳米颗粒临床进展不如LNP,但聚合物具有与脂质相似的优势,能够有效传递mRNA,阳离子聚合物将核酸浓缩成具有不同形状和大小的复合物,可通过内吞作用进入细胞。
聚乙烯亚胺是研究最广泛的核酸传递聚合物,尽管其功效卓越,但由于其高电荷密度以及毒性限制了应用。
新型含脂聚合物电荷改变可释放转运体(CARTs)能有效地靶向T细胞,操纵T细胞是非常困难的,因此,CART是一种极具吸引力的传递材料,在mRNA疫苗和基因治疗领域具有巨大潜力。
多肽也可以将mRNA传递到细胞中,这要归功于其主链和侧链中的阳离子或两亲胺基,这些阳离子或两亲胺基与mRNA静电结合并形成纳米复合物。
角鲨烯阳离子纳米乳液也可以传递mRNA,这些纳米乳剂由油性角鲨烯核组成,不过角鲨烯基阳离子纳米乳剂从内涵体逃逸并将mRNA输送到细胞质中的机制尚不清楚。
有了这些日渐成熟的递送技术,mRNA癌症疫苗开发到什么程度了?
3巨头时代来临
实际上,mRNA三大巨头BioNTech、Moderna、CureVac以及国内的一些mRNA企业,早在开发新冠疫苗之前,主要都将治疗性的癌症疫苗作为各自mRNA技术的核心项目进行推进。
从研发现状来看,mRNA疫苗已被广泛尝试应用于包括前列腺癌、急性骨髓白血病、转移黑色素瘤、成神经细胞瘤等多种类型肿瘤的治疗研究。
据统计,BioNTech拥有超过30个产品管线,肿瘤相关的约15个,其正在开发针对直肠癌、黑色素瘤和其他癌症类型的治疗方法。其中针对晚期黑色素瘤和HPV16阳性头颈癌的BNT111和BNT113产品已经进入临床II期,针对病人来源特异性抗原的个性化癌症疫苗BNT122也已经进入临床I、II期。2021年11月,BioNTech发布公告宣布美国FDA授予了其mRNA癌症疫苗BNT111快速通道资格。
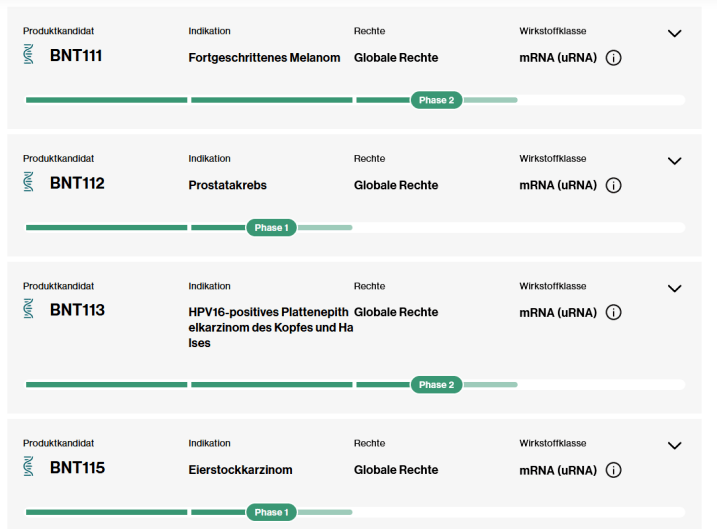
▲BioNTech部分mRNA研发管线?来源:BioNTech官网
Moderna同样处于竞速中。Moderna目前产品线合计超过45个,与肿瘤相关的约5个。其中有一款个性化的癌症疫苗mRNA-4157,能够容纳高达34个编码新抗原的mRNA序列,针对多个癌种,在临床I期的疾病控制率达到了90%,目前正在进行临床II期试验。
今年10月,Moderna宣布与默沙东合作,将联合开发并销售一种个性化精准治疗癌症疫苗,推动Moderna的mRNA技术与默沙东PD-1 Keytruda联用,探索治疗高危黑色素瘤患者。目前,该项目处于临床试验II期,共招募了157例受试者。
CureVac专注于开发针对肿瘤、罕见病和传染性疾病的mRNA疗法,已有14个候选药物,其中9款候选药物已经进入了临床阶段。其中,CV-8102是一款基于RNA的单链非编码TLR-7/8和RIG-1激动剂,早在2017年就已开展了I期临床研究,用于晚期黑色素瘤、皮肤鳞状细胞癌、头颈部鳞状细胞癌或腺样囊性癌患者的治疗。
但是目前全球范围内大部分mRNA癌症疫苗管线的研发都还处于较早阶段,基础性研究也尚未完全成熟,中国企业还是有很大的机会实现弯道超车。
4能否弯道超车?
2022年11月11日,中国科学院国家纳米科学中心王海研究团队在Advanced Functional Materials期刊发表了一篇研究论文。该研究开发了一种水凝胶-LNPs系统(HA-mRLNPs),可以有效地将编码肿瘤抗原的mRNA递送到树突状细胞进行抗原呈递,诱导抗原特异性CD8+T细胞杀伤肿瘤细胞,而且可在室温下储存。该研究证明稳定和持久免疫水凝胶-LNPs体系可用于有效的肿瘤免疫治疗。
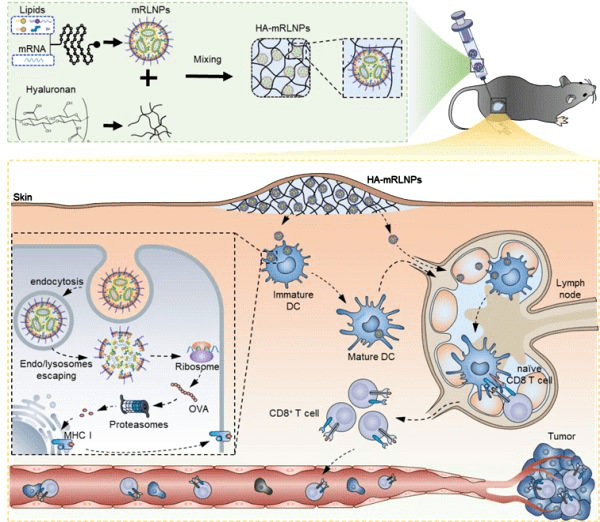
▲水凝胶-LNPs系统制备和体内肿瘤免疫示意图?来源:参考资料7
这项研究的出现也证明了我国完全有能力在mRNA的基础性研究中取得突破。
据不完全统计,我国专注mRNA技术开发的至少有26家,这一数量正在急剧增加。其中实力领先且临床试验进度靠前的公司包括艾博生物、斯微生物、丽凡达/艾美疫苗、深信生物、尧唐生物、嘉晨西海、瑞吉生物、蓝鹊生物等。
艾博生物成立于2019年,拥有业界领先并具有自主知识产权的mRNA和纳米递送技术平台,自主研发的动态精准混合技术可适用于纳米脂球的工业化生产。目前进展最快的一款mRNA疫苗为艾博生物联合沃森生物、军事科学院医学研究院共同研发mRNA新冠疫苗ARCoV,已于2022年9月获印度尼西亚食品药品监督管理局(BPOM)颁发紧急用途许可证,这是艾博生物在海外获得的第一个EUA,也是中国首款在国际上获批的mRNA疫苗。
不过目前艾博生物研发管线中主要为预防性病毒疫苗,尚未见到布局mRNA癌症疫苗进入临床阶段。但在艾博生物的公开介绍中表示,癌症疫苗是艾博生物在肿瘤领域产品开发的一个最为重要、也是目前项目占比最大的方向。
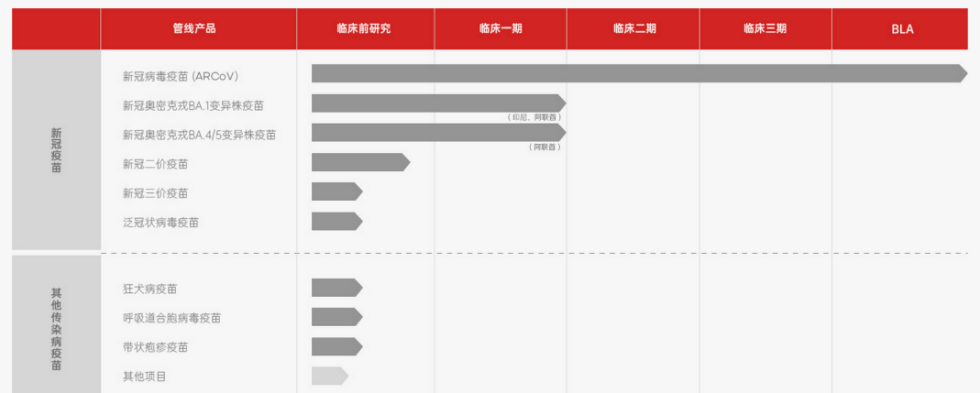
▲艾博生物研发管线?来源:艾博生物官网
斯微生物2016年5月成立于上海张江,2017年获得休斯顿卫理会医院授权LPP递送平台全球独家商业化权益,2018年建成mRNA生产中心,完成mRNA合成平台验证、纳米制剂产业化生产验证。今年10月,斯微生物宣布其自主研发的mRNA新冠疫苗三期临床试验已在老挝正式启动。关于癌症疫苗的研发进展,斯微生物透露,目前其mRNA个性化癌症疫苗已在澳大利亚开展I期临床,这是国内第一家进入临床的个性化癌症疫苗。
嘉晨西海成立于2019年,是国内mRNA行业中工业经验尤其是CMC方面经验领先的一家公司,管线涵盖肿瘤免疫治疗、传染病疫苗、罕见病和医学美容,其中自复制mRNA癌症疫苗项目JCXH-211和JCXH-212分别在美国和中国进行I/II期临床试验。
总的来看,国内的mRNA癌症疫苗领域从数量来讲还不能构成竞争关系,更多的是在共同推动mRNA癌症疫苗的应用与发展,处于努力把管线推进到临床应用的初始阶段。而一些国内Big Pharma的入场支持,如石药集团等,或许更多的只是看中mRNA新冠疫苗的短期收益,而非真正想要投入mRNA技术的发展。
—?结语?—
未来,mRNA技术在癌症疫苗研发方面的成果是非常值得期待的,新冠疫情给了mRNA一次千载难逢的机会,在行业领先者们获得巨大的收益后,对mRNA的投入也将会史无前例。假设2030年便能看到mRNA癌症疫苗的成果,那将是人类医疗史上最伟大的时刻之一。
国内在mRNA技术的发展中,切忌目光短浅,mRNA并非只有做新冠疫苗才是唯一出路。只有真正投入到基础性的研究中去,才有实现弯道超车的可能。但很遗憾,目前国内无论Biotech还是Big Pharma当下的重心都不在此,如果不尽力弥补技术上的差距,就算mRNA的下一个风口来了,国内企业也很难把握得住。
参考文献:
1、《十年磨一剑:mRNA疫苗诞生史》,生物世界,2021-1-27
2、《用于肿瘤&罕见病治疗的mRNA药物有哪些?》,药投圈,2020-12-16
3、《柳叶刀综述:mRNA癌症疫苗的递送及临床进展》,金斯瑞生物官微,2022-11-7
4、《癌症疫苗即将问世:能否一针清除癌细胞?哪些药企在布局?》,澎湃,2022-10-18
5、《癌症疫苗8年内面世?mRNA强在哪,国内药企回应最新进展》,新浪财经,2022-10-18
6、《mRNA疫苗行业分析报告》,佰傲谷,2022-10-27
7、《国家纳米中心王海团队在肿瘤纳米疫苗中取得新突破》,生物世界,2022-11-23
版权声明:除特殊说明外,本站所有文章均为 字节点击 原创内容,采用 BY-NC-SA 知识共享协议。原文链接:https://byteclicks.com/44082.html 转载时请以链接形式标明本文地址。转载本站内容不得用于任何商业目的。本站转载内容版权归原作者所有,文章内容仅代表作者独立观点,不代表字节点击立场。报道中出现的商标、图像版权及专利和其他版权所有的信息属于其合法持有人,只供传递信息之用,非商务用途。如有侵权,请联系 gavin@byteclicks.com。我们将协调给予处理。
赞
